LA FDA OTORGA LA DESIGNACIÓN DE DISPOSITIVO INNOVADOR PARA EL GLOBO ORBERA DE APOLLO PARA EL TRATAMIENTO DE NASH
- Jue 4 de Mar 2021
- Sochob
- Noticias Actuales
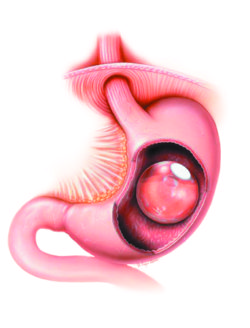
Apollo Endosurgery ha recibido una designación de dispositivo innovador de la FDA para el balón intragástrico Orbera, específicamente para la indicación de uso en el tratamiento de pacientes con IMC entre 30 – 40 kg/m2 con esteatohepatitis no alcohólica no cirrótica (NASH) con fibrosis hepática.
El Programa de dispositivos innovadores de la FDA tiene como objetivo ayudar a los pacientes a recibir un acceso más oportuno a tecnologías innovadoras que tienen el potencial de proporcionar un tratamiento o diagnóstico más eficaz para enfermedades o afecciones que amenazan la vida o debilitan de forma irreversible.
«Orbera ha demostrado constantemente, tanto en el estudio fundamental como en el estudio de aprobación posterior a la comercialización, la capacidad de ayudar a los pacientes a perder un promedio de 7-10% de pérdida de peso corporal total (TBWL) durante 6-12 meses, lo que es significativamente mayor que la modificación del estilo de vida por sí sola», dijo Dr. Christopher Gostout, director médico de Apollo Endosurgery. «La literatura y el estudio IDE de Mayo sugieren que estos niveles de pérdida de peso pueden tener un efecto positivo en la resolución o el retraso de la progresión de la EHGNA. Con la designación de avance, podremos construir aún más el cuerpo de evidencia clínica y buscar la expansión de la etiqueta para el uso de Orbera para pacientes con NASH».
La esteatohepatitis no alcohólica (NASH) es una forma grave de enfermedad del hígado graso, que se asocia con inflamación del hígado y puede progresar a cirrosis e insuficiencia hepática. Los pacientes con EHGNA tienen un mayor riesgo de morbilidad y mortalidad por causas relacionadas con el hígado, y la EHGNA es una de las tres principales afecciones que conducen al trasplante de hígado. La población adulta con EHGNA de EEUU que tiene un IMC entre 30 – 40 kg/m2 es aproximadamente 10 millones, y aunque actualmente no existen tratamientos aprobados por la FDA para la EHGNA, la pérdida de peso es el tratamiento recomendado y esencial para una mejora significativa de ella.
Las pautas de tratamiento actuales apuntan a un 7 – 10% de pérdida de peso corporal total (TBWL). Con este grado de pérdida de peso, las características histológicas de la EHNA mejoran en un porcentaje significativo de pacientes, con resolución de la inflamación hepática, salida de grasa del hígado, y regresión de la fibrosis con el tiempo. Sin embargo, los pacientes generalmente no logran estos niveles requeridos de pérdida de peso utilizando solo los programas de control del estilo de vida.
Orbera es una solución de pérdida de peso no quirúrgica y sin incisiones diseñada para pacientes adultos que padecen obesidad, que no son apropiados para la cirugía o que no la están considerando, pero para quienes la dieta, el ejercicio o las intervenciones farmacéuticas no han funcionado. Una vez que el globo está en su lugar, el paciente trabaja con su médico y su personal en un programa formal de modificación del estilo de vida para alcanzar sus objetivos de pérdida de peso a largo plazo. El entrenamiento se lleva a cabo durante 12 meses mientras el globo está en su lugar. El programa está diseñado para ayudar al paciente a desarrollar hábitos saludables y sostenibles que ayudarán a mantener el peso perdido con el tiempo.
El estudio de la Clínica Mayo aprobado por IDE (G160077) se diseñó explícitamente para evaluar los efectos de la colocación de Orbera en las características metabólicas e histológicas de NASH, incluido el NAS (que indica la resolución de la grasa y la inflamación en el hígado) y la puntuación de fibrosis. Hubo una mejora notable en estas medidas de resultado de NASH cuando se eliminó Orbera después de seis meses. Específicamente:
- La puntuación de actividad de la enfermedad del hígado graso no alcohólico (NAS) mejoró en 18/20 pacientes (90%) y en 16/20 (80%) de los pacientes disminuyó en ≥ 2 puntos.
- El 15% tuvo regresión histológica de la fibrosis (cicatrización) y elastografía por resonancia magnética (MRE): la fibrosis detectada mejoró en el 50% (10/20) de los pacientes.
Si bien Orbera ha sido aprobado por la FDA desde 2015 para la pérdida de peso, la concesión de la designación de dispositivo innovador es un importante paso adelante para abordar potencialmente una importante necesidad insatisfecha de mejorar la salud de los pacientes con NASH.
Fuente: http://www.bariatricnews.net
Referencias: https://www.niddk.nih.gov/health-information/liver-disease/nafld-nash
Bazerbachi F, Vargas EJ, Rizk M, et al. Intragastric balloon placement induces significant metabolic and histologic improvement in patients with nonalcoholic steatohepatitis. Clin Gastroenterol Hepatol 2021;19:146-154..
