OBESIDAD, INFLAMACIÓN Y COMORBILIDADES
- Mié 30 de Sep 2009
- Sochob
- Tema del Mes (Archivo)
Curso Educación Continua en Obesidad 2009
Resumen clase Dr Alex Valenzuela
La inflamación, definida como una respuesta defensiva inespecífica contra una noxa (infección, traumatismo, etc), es considerada cuando esta es crónica,como un importante factor contribuyente a muchas patologías metabólicas y no metabólicas, entre las cuales destacan ; diabetes tipo 2, hipertensión arterial,dislipidemia, enfermedades neurodegenerativas y autoinmunes.
La respuesta inflamatoria se caracteriza por la producción de una serie de sustancias químicas sintetizadas por múltiples células, en especial glóbulos blancos e hígado (proteínas o reactantes de fase aguda), destinadas a radicar el agente agresor y a la reparación de tejidos.
(Tabla 1).

Una de las maneras rápidas y fáciles de observar la inflamación en nuestro cuerpo, es a través de la medición de marcadores inflamatorios, dentro de los cuales destaca la proteína C reactiva ultrasensible (PCR), examen capaz de cuantificar niveles mínimos circulantes de PCR y evidenciar grados leves de inflamación, como los observados en la obesidad. Valores plasmáticos de CRP > 3 mg/L son considerados de alto riesgo de enfermedad cardiovascular, entre 2 y 3 mg/L de riesgo intermedio y menores de 1 mg/L normales y de bajo riesgo cardiovascular.
Los obesos exhiben niveles circulantes incrementados de CRP ultrasensible en concordancia con el grado de adiposidad, lo cual ha sido observado tanto en adultos como en niños.
Tejido adiposo órgano endocrino
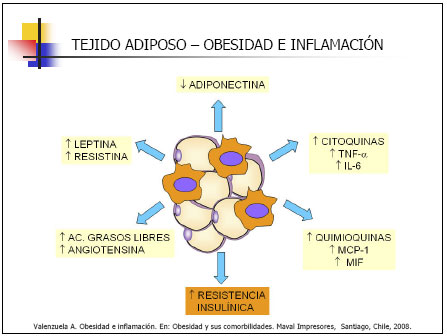
En los últimos años, el tejido adiposo ha pasado de ser un simple órgano almacenador de energía a ser un importante órgano endocrino, secretando una gran cantidad de hormonas, citoquinas, factores de crecimiento y quimioquinas, denominadas colectivamente como adipoquinas, que actuando de manera autocrina, paracrina y endocrina participan activamente no solo en el desarrollo y metabolismo del tejido adiposo, sino que también en múltiples funciones biológicas, tales como la reproducción, la inmunidad, la pubertad, regulación endocrina y presión arterial.
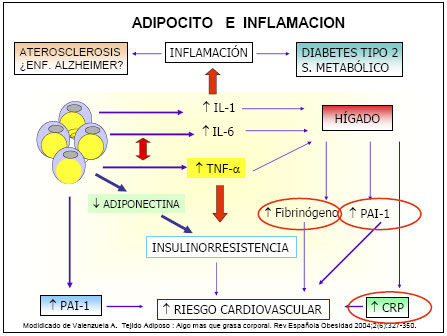
En la obesidad, la producción de adipoquinas se encuentra incrementada de manera anormal, secretando una mayor cantidad de adipoquinas a la circulación, la mayor parte de ella con características inflamatorias (factor de necrosis tumoral alfa, interleuquina 6, inhibidor del activador del plasminógeno- 1 (PAI-1, resistina, etc), lo que determina que la obesidad sea considerada hoy un estado inflamatorio crónico leve. La inflamación del tejido adiposo en la obesidad tiene un significativo y amplio impacto sobre la glucosa, lípidos y el metabolismo energético, además de incrementar el riesgo de desarrollar múltiples patologías, especialmente de tipo cardiovascular.
Macrófagos principales responsables
El tejido adiposo está constituido por adipocitos, preadipocitos, leucocitos, células endoteliales, mesenquimáticas y neuronales. En condiciones normales el tejido adiposo contiene una cantidad pequeña de macrófagos residentes, los cuales tienen funciones protectoras, incluyendo reparación tisular y producción de citoquinas antiinflamatorias (IL-10), no obstante en la medida que este empieza a expandirse, como ocurre en la obesidad, se incrementa notoriamente el reclutamiento de macrófagos proveniente de la circulación, estando su cantidad en directa relación con el índice de masa corporal, tamaño adipocitario e insulinorresistencia, los cuales tienen un perfil secretorio diferente a los macrófagos residentes. Son estos macrófagos que infiltran el tejido adiposo en la medida que se desarrolla la obesidad, los principales responsables de la generación de citoquinas que promueven la inflamación, sinergizando con la producción por parte de los adipocitos, que es en mucho menor cuantía.
Posibles explicaciones para el reclutamiento de macrófagos en tejido adiposo No se sabe con exactitud que determina la llegada de macrófagos circulantes (monocitos) al tejido adiposo, pero no se descarta que su origen sea multifactorial y algunas posibles explicaciones han sido formuladas:
a) Apoptosis adipocitaria: Es una de las hipótesis más aceptadas y señala que la llegada de macrófagos al tejido adiposo sería secundaria a la muerte adipocitaria y que la liberación de fragmentos adipocitarios serían los causantes de la atracción de macrófagos, ya que los macrófagos se ubican preferentemente alrededor de adipocitos muertos.
Esta muerte de adipocitos sería por un déficit de irrigación sanguínea (hipoxia).
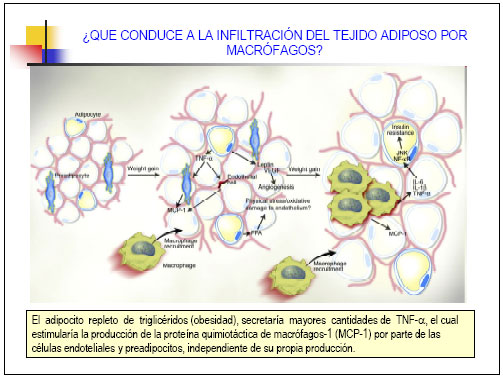
b) Proteína quimiotáctica de macrófagos-1 (MCP-1); La MCP-1 es una quimioquina (mólecula que atrae a otras células hacia el sitio de daño o infección, en este caso monocitos que son los precursores de los macrófagos) que es sintetizada por macrófagos, células endoteliales y adipocitos, estando su expresión estrechamente relacionada con el número de macrófagos reclutados. Dado que la síntesis de MCP-1 está incrementada en el tejido adiposo del obeso, no se descarta que este aumento sea uno de los estímulos que atrae macrófágos hacia él.
Implicancias del estado inflamatorio crónico leve en la obesidad
La síntesis de adipoquinas proinflamatorias por parte del tejido adiposo, particularmente por los macrófagos, produce una gran cantidad de acciones negativas, destacando la generación de insulinorresistencia. Tanto el TNF-α como la IL-6, han sido implicados en la producción de insulinorresistencia, encontrándose sus concentraciones plasmáticas aumentadas en la obesidad. Por tanto este estado inflamatorio crónico leve favorece la aparición de todas las patologías asociadas con la insulinorresistencia, en especial la diabetes tipo 2, ya que ambas adipoquinas alteran la vía de señalamiento intracelular de la insulina, especialmente inhibiendo el funcionamiento del sustrato para el receptor de insulina 1 o 2 (IRS-1/2), impidiendo con ello la translocación de los transportadores de glucosa-4 (Glut4) y por ende la incorporación de la glucosa al interior de la célula.
Adiponectina y su acción antiinflamatoria
La hormona adiponectina normalmente es la adipoquina más abundantemente secretada por el tejido adiposo (adipocito), cuyas concentraciones plasmáticas fluctúan entre 5 -30 ug/ml, no obstante que en la obesidad (y diabetes tipo 2) su síntesis se encuentra disminuida, probablemente por inhibición de su síntesis adipocitaria dado por el TNF-α. En general en todos los estados que cursan con insulinorresistencia sus concentraciones plasmáticas se encuentran disminuidas y bajos niveles circulantes son considerados hoy un factor de riesgo para el desarrollo de diabetes tipo 2 y enfermedad cardiovascular. Por el contrario, niveles incrementados de adiponectina se asocian positivamente con insulinosensibilidad y mejoría de la homeostasis glucosídica.
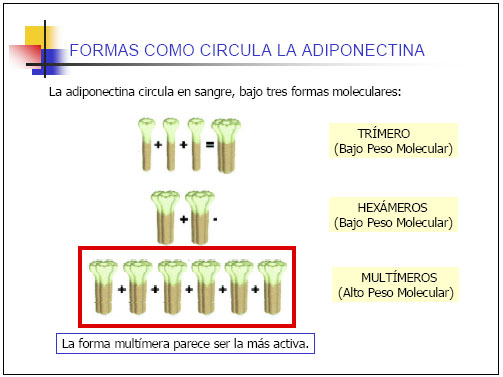
La adiponectina tiene acciones insulinosensibilizantes, antiaterogénicas, antitumorales y antiinflamatorias, circulando bajo diversas formas moleculares, trímeros (bajo peso molecular), hexámeros (peso molecular intermedio) y multímeros (de alto peso molecular), siendo esta última forma la más activa biológicamente.
Fármacos antiinflamatorios e insulinorresistencia
Numerosos fármacos han demostrado tener acciones antiinflamatorias y mejorar por ende la insulinorresistencia y la aterosclerosis, reduciendo el riesgo de diabetes tipo 2 y enfermedad cardiovascular, tales como son el ácido acetilsalicílico, las estatinas, bloqueadores del sistema renina-angiotensina y glitazonas (rosiglitazona y pioglitazona), en gran parte por inhibir la activación del factor nuclear kappa B (NF-κB), un factor de transcripción que promueve la síntesis de citoquinas proinflamatorias.
Dosis elevadas de aspirina (7 g diarios) han demostrado reducir significativamente los niveles de glicemia en pacientes diabéticos y dosis baja de aspirina administrada de manera crónica a sujetos sanos se acompaña de una disminución del riesgo de desarrollar diabetes.
Las estatinas actúan disminuyendo la inflamación por reducir la activación del factor de transcripción nuclear kappa B (NF-κ B), el cual incrementa la expresión de múltiples moléculas proinflamatorias (TNF-α, IL-6, MCP-1) y la CRP.
REFERENCIAS
Fantuzzi G. Adiponectin and inflammation: consensus and controversy. J Allergy Clin Immunol 2008;121:326–330.
Ferrante AW Jr. Obesity-induced inflammation: a metabolic dialogue in the language of inflammation. J Intern Med 2007;262:408–414.
Hayashino Y, Hennekens CH, Kurth T. Aspirin use and risk of type 2 diabetes in apparently healthy men. Am J Med 2009;122:374–379.
Hotamisligil GS. Inflammation and metabolic disorders. Nature 2006;444: 860–867.
Hundal RS, et al. Mechanism by which high-dose aspirin improves glucose metabolism in type 2 diabetes. J Clin Invest 2002;109:1321–1326.
Lazar MA. How obesity causes diabetes: not a tall tale. Science 2005;307:373–375
Strissel KJ, Stancheva Z, Miyoshi H, et al. Adipocyte death, adipose tissue remodeling, and obesity complications. Diabetes 2007;56:2910–2918.
Valenzuela A. Obesidad e inflamación. En: Obesidad y sus comorbilidades. Maval Impresores, Santiago, Chile, 2008.
Weisberg SP, McCann D, Desai M, et al. Obesity is associated with macrophage accumulation in adipose tissue. J Clin Invest 2003;112:1796–1808.
Weyer C, Funahashi T, Sachiyo T et al. Hypoadiponectinemia in obesity and type 2 diabetes: close association with insulin resistance and hyperinsulinemia.
J Clin Endocrinol Metab 2001;86:1930–1935.
Ye J. Emerging role of adipose tissue hypoxia in obesity and insulin resistance.
Int J Obes 2008:33;54-66.
Xu H, et al. Chronic inflammation in fat plays a crucial role in the development
of obesity-related insulin resistance. J Clin Invest 2003;112:1821–1830
Artículos Anteriores
Obesidad: Una mirada más allá de la sobrealimentación y el sedentarismo.
Visfatina: Una puesta al día
Diabetes e Hipogonadismo Hipogonadotrófico
